السيلينيوم (Se)، عنصر كيميائي في مجموعة الأكسجين (المجموعة 16 [VIa] من الجدول الدوري) ، يرتبط ارتباطًا وثيقًا بالخصائص الكيميائية والفيزيائية مع عناصر الكبريت والتيلوريوم. السيلينيوم نادر ، فهو يؤلف ما يقرب من 90 جزءًا لكل مليار من قشرة الأرض. يتم العثور عليها أحيانًا غير مجمعة ، مصاحبة للكبريت الأصلي ، ولكن غالبًا ما توجد مع المعادن الثقيلة (النحاس أو الزئبق أو الرصاص أو الفضة) في عدد قليل من المعادن. المصدر التجاري الرئيسي للسيلينيوم هو منتج ثانوي لتكرير النحاس ؛ استخداماتها الرئيسية هي في تصنيع المعدات الإلكترونية والأصباغ وصناعة الزجاج. السيلينيوم هو معدن (عنصر وسيط في الخصائص بين المعادن واللافلزات). الشكل المعدني الرمادي للعنصر هو الأكثر استقرارًا في ظل الظروف العادية ؛ هذا النموذج له خاصية غير عادية لزيادة الموصلية الكهربائية بشكل كبير عند تعرضه للضوء. مركبات السيلينيوم سامة للحيوانات ؛ النباتات التي تزرع في تربة ذات حشرات قد تركز العنصر وتصبح سامة.
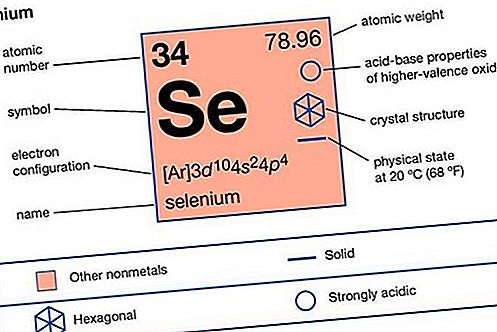

عنصر مجموعة الأكسجين: التواجد والاستخدامات الطبيعية
عنصر السيلينيوم (الرمز Se) أكثر ندرة من الأكسجين أو الكبريت ، ويضم حوالي 90 جزءًا لكل مليار من القشرة
.خصائص العنصر
| العدد الذري | 34 |
|---|---|
| الوزن الذري | 78.96 |
| كتل النظائر المستقرة | 74 ، 76 ، 77 ، 78 ، 80 ، 82 |
| نقطة الانصهار | |
| عديم الشكل | 50 درجة مئوية (122 درجة فهرنهايت) |
| اللون الرمادي | 217 درجة مئوية (423 درجة فهرنهايت) |
| نقطة الغليان | 685 درجة مئوية (1،265 درجة فهرنهايت) |
| كثافة | |
| عديم الشكل | 4.28 جرام / سم 3 |
| اللون الرمادي | 4.79 جرام / سم 3 |
| الأكسدة | −2 ، +4 ، +6 |
| التوزيع الإلكترون | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 4 |
التاريخ
في عام 1817 ، لاحظ الكيميائي السويدي Jöns Jacob Berzelius مادة حمراء ناتجة عن خامات كبريتيد من مناجم فالون ، السويد. عندما تم التحقيق في هذه المادة الحمراء في العام التالي ، ثبت أنها عنصر وتم تسميتها بعد القمر أو إلهة القمر سيلين. اكتشف Berzelius خامًا يحتوي على نسبة عالية من السيلينيوم بشكل غير عادي قبل أيام فقط من تقديم تقريره إلى الجمعيات العلمية في العالم بشأن السيلينيوم. يتضح حس الدعابة لديه في الاسم الذي أعطاه خام اليوكاريت ، بمعنى "في الوقت المناسب".
حدوث واستخدامات
تبلغ نسبة السيلينيوم في قشرة الأرض حوالي 10 −5 إلى 10 −6 بالمائة. تم الحصول عليها بشكل رئيسي من الأوحال الأنود (الرواسب والمواد المتبقية من الأنود) في التكرير الإلكتروليتي للنحاس والنيكل. المصادر الأخرى هي غبار المداخن في إنتاج النحاس والرصاص والغازات المتكونة في بيريت التحميص. يرافق السيلينيوم النحاس في تكرير هذا المعدن: قد يتركز حوالي 40 في المائة من السيلينيوم الموجود في الخام الأصلي في النحاس المودع في العمليات الإلكتروليتية. يمكن الحصول على حوالي 1.5 كيلوغرام من السيلينيوم من طن من النحاس المصهور.
عند دمجها بكميات صغيرة في الزجاج ، يعمل السيلينيوم كمزيل للون. بكميات أكبر يضفي على الزجاج لون أحمر واضح مفيد في أضواء الإشارة. يتم استخدام العنصر أيضًا في صنع المينا الحمراء للسيراميك والأدوات الفولاذية ، بالإضافة إلى تقسية المطاط لزيادة مقاومة التآكل.
جهود تنقية السيلينيوم هي الأكبر في ألمانيا واليابان وبلجيكا وروسيا.
التآصل
تآثرات السيلينيوم ليست واسعة مثل الكبريت ، ولم يتم دراسة التآثرات بدقة. يتكون نوعان بلوريان فقط من السيلينيوم من جزيئات حلقي Se 8: تسمى α و β ، وكلاهما موجود كبلورات أحادية اللون أحادية. يتم تشكيل مؤثرات رمادية ذات خصائص معدنية عن طريق الحفاظ على أي من الأشكال الأخرى عند 200-220 درجة مئوية وهي الأكثر استقرارًا في الظروف العادية.
ينتج شكل غير متبلور (غير متبلور) ، أحمر ، مسحوق من السيلينيوم عندما يتم معالجة محلول حمض سيليني أو أحد أملاحه بثاني أكسيد الكبريت. إذا كانت الحلول مخففة للغاية ، فإن الجزيئات الدقيقة للغاية من هذا الصنف تنتج تعليقًا غروانيًا أحمر شفافًا. ينتج الزجاج الأحمر الشفاف عن عملية مشابهة تحدث عندما تتم معالجة الزجاج المنصهر المحتوي على السيلينيت بالكربون. يتم تشكيل مجموعة متنوعة من السيلينيوم الزجاجي والأسود تقريبًا عن طريق التبريد السريع للتعديلات الأخرى من درجات حرارة أعلى من 200 درجة مئوية. يتم تحويل هذا الشكل الزجاجي إلى التآزر الأحمر البلوري عند تسخينه فوق 90 درجة مئوية أو عند إبقائه على اتصال بالمذيبات العضوية ، مثل الكلوروفورم أو الإيثانول أو البنزين.
تجهيز
يتم الحصول على السيلينيوم النقي من الوحل والوحل المتكون في إنتاج حامض الكبريتيك. يذوب السيلينيوم الأحمر النجس في حمض الكبريتيك في وجود عامل مؤكسد ، مثل نترات البوتاسيوم أو بعض مركبات المنغنيز. يتم تكوين كل من حمض السيلينيوم ، H 2 SeO 3 ، وحمض السيلينيوم ، H 2 SeO 4 ، ويمكن ترشيحهما من المواد غير القابلة للذوبان المتبقية. تستخدم الطرق الأخرى الأكسدة عن طريق الهواء (التحميص) والتسخين مع كربونات الصوديوم لإعطاء سيلينيت الصوديوم القابل للذوبان ، Na 2 SeO 3 · 5H 2 O ، وسيلينات الصوديوم ، Na 2 SeO 4. يمكن استخدام الكلور أيضًا: ينتج تأثيره على سيلينيدات المعادن مركبات متطايرة بما في ذلك ثنائي كلوريد السيلينيوم ، SeCl 2 ؛ رابع كلوريد السيلينيوم ، SeCl 4 ؛ ثنائي كلوريد ثنائي الصوديوم ، Se 2 Cl 2 ؛ وأكسيد كلوريد السيلينيوم ، SeOCl 2. في إحدى العمليات ، يتم تحويل مركبات السيلينيوم هذه عن طريق الماء إلى حمض السيلينيوم. يتم استرداد السيلينيوم أخيرًا عن طريق معالجة حمض السيلينيوم بثاني أكسيد الكبريت.
السيلينيوم هو عنصر شائع من الخامات يتم تقييمه لمحتواه من الفضة أو النحاس. يصبح مركزًا في الوحل المتراكم أثناء التنقية الإلكتروليتية للمعادن. تم تطوير طرق لفصل السيلينيوم عن هذه الأوحال ، والتي تحتوي أيضًا على بعض الفضة والنحاس. يشكل ذوبان الوحل سلينيد الفضة ، Ag 2 Se ، وسيلينيد النحاس (I) ، Cu 2 Se. يعالج علاج هذه السيلينيدات بحمض هيبوكلوروس ، HOCl ، سيلينات قابلة للذوبان وسيلينات ، والتي يمكن تقليلها باستخدام ثاني أكسيد الكبريت. يتم تحقيق التنقية النهائية للسيلينيوم عن طريق التقطير المتكرر.
الخواص الفيزيائية - الكهربائية
إن الخاصية الفيزيائية الأكثر تميزًا للسيلينيوم البلوري هي الموصلية الضوئية: عند الإضاءة ، تزيد الموصلية الكهربائية أكثر من 1000 مرة. تنجم هذه الظاهرة عن تعزيز أو إثارة الإلكترونات غير النظيفة نسبيًا عن طريق الضوء إلى حالات الطاقة الأعلى (تسمى مستويات التوصيل) ، مما يسمح بهجرة الإلكترون ، وبالتالي التوصيل الكهربائي. على النقيض من ذلك ، فإن إلكترونات المعادن النموذجية موجودة بالفعل في مستويات التوصيل أو النطاقات ، قادرة على التدفق تحت تأثير قوة كهربائية.
تختلف المقاومة الكهربائية للسيلينيوم على مدى هائل ، اعتمادًا على متغيرات مثل طبيعة التآثر ، والشوائب ، وطريقة التكرير ، ودرجة الحرارة ، والضغط. معظم المعادن غير قابلة للذوبان في السيلينيوم ، وتزيد الشوائب اللافلزية من المقاومة.
إن إضاءة السيلينيوم المتبلور لمدة 0.001 ثانية تزيد من توصيله بعامل 10 إلى 15 مرة. الضوء الأحمر أكثر فعالية من الضوء ذو الطول الموجي الأقصر.
يتم الاستفادة من هذه الخصائص الكهروضوئية والحساسية للضوء للسيلينيوم في بناء مجموعة متنوعة من الأجهزة التي يمكن أن تترجم الاختلافات في شدة الضوء إلى التيار الكهربائي ومن ثم إلى التأثيرات البصرية أو المغناطيسية أو الميكانيكية. تعتمد أجهزة الإنذار وأجهزة الفتح والإغلاق الميكانيكية وأنظمة السلامة والتلفزيون والأفلام الصوتية والتصوير بالأشعة السينية على خاصية أشباه الموصلات والحساسية الضوئية للسيلينيوم. تم تصحيح التيار الكهربائي المتناوب (التحويل إلى التيار المباشر) لسنوات بواسطة الأجهزة التي تتحكم فيها السيلينيوم. تم استبدال العديد من تطبيقات الخلايا الكهروضوئية التي تستخدم السيلينيوم بأجهزة أخرى تستخدم مواد أكثر حساسية ومتوفرة بسهولة وأكثر سهولة في التصنيع من السيلينيوم.