أنهيدريد ، أي مركب كيميائي يتم الحصول عليه ، سواء من الناحية العملية أو من حيث المبدأ ، بالقضاء على الماء من مركب آخر. أمثلة على أنهيدريد غير عضوي هي ثالث أكسيد الكبريت ، SO 3 ، المشتق من حمض الكبريتيك ، وأكسيد الكالسيوم ، CaO ، المشتق من هيدروكسيد الكالسيوم. غالبًا ما تسمى ثالث أكسيد الكبريت وأكاسيد أخرى تتكون عن طريق إزالة الماء من حمض أنهيدريد الحمضي ، في حين أن تلك مثل أكسيد الكالسيوم التي تنتجها قاعدة عند فقدان الماء يتم تعيينها أنهيدريد أساسي.
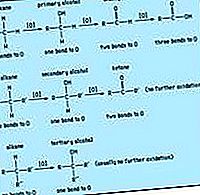
حمض الكربوكسيل: الأنهيدريد
المجموعة الوظيفية من أنهيدريد كربوكسيل هي مجموعتان أسيل مرتبطتان بذرة أكسجين. قد يكون أنهيدريد متماثل (اثنان متطابقان
أهم أنهيدريد عضوي هو أنهيدريد أسيتيك (CH 3 CO) 2 O. يتم تحضيره صناعيًا بإحدى طريقتين: عن طريق أكسدة الأسيتالديهيد الجوي في وجود أسيتات فلزية ؛ ومن حمض الأسيتيك عن طريق التفاعل مع الأسيتيلين أو الكيتين. يمكن تحضير الأنهيدريدات العضوية الأخرى من أحماض كربوكسيلية عن طريق التفاعل مع أنهيدريد الخل أو الكيتين أو ميثوكسي أسيتيلين أو أسيتات الأيزوبروبينيل. يتم إنتاج الأنهيدريد أيضًا عندما تتفاعل هاليدات الأسييل مع أنهيدريد الخل أو مع حمض الكربوكسيل والبيريدين.
يتم استخدام الأنهيدريد العضوي لإدخال مجموعة الأسيل (RCO) في التوليف العضوي. تتفاعل مع الماء لإعطاء الأحماض الكربوكسيلية ، مع الكحول أو الفينول لإعطاء الإسترات ، ومع الأمونيا والأمينات لإعطاء أميدات. يستخدم أنهيدريد الخل في تصنيع أسيتات السليلوز ، والذي يستخدم على نطاق واسع كقاعدة للشريط المغناطيسي وفي تصنيع ألياف النسيج. أيضا ، يتم تسخينه بحمض الساليسيليك لإنتاج حمض أسيتيل الساليسيليك الكيميائي (الأسبرين).