الفينول فورمالدهايد
كثير من الناس يؤرخون بداية صناعة البلاستيك الحديثة إلى عام 1907 ، عندما تقدم ليو هندريك بايكلاند ، الكيميائي الأمريكي البلجيكي المولد ، بطلب للحصول على براءة اختراع على مادة حرارية من الفينول فورمالدهايد أصبحت تعرف في النهاية باسم العلامة التجارية الباكليت. تُعرف أيضًا باسم راتنجات الفينول ، وكانت بوليمرات الفينول فورمالدهايد أول البوليمرات الاصطناعية بالكامل التي يتم تسويقها. على الرغم من أن المنتجات المقولبة لم تعد تمثل أهم تطبيقاتها ، إلا أنها من خلال استخدامها كمادة لاصقة فإنها لا تزال تمثل ما يقرب من نصف إجمالي إنتاج البوليمرات الحرارية.
كانت التجارب مع الراتنجات الفينولية سبقت بالفعل عمل بايكلاند. في عام 1872 قام الكيميائي الألماني Adolf von Baeyer بتكثيف الفينول ثلاثي الوظائف والفورمالديهايد متعدد الوظائف ، وفي العقود اللاحقة قام طالب Baeyer Werner Kleeberg والكيميائيون الآخرون بالتحقيق في المنتجات ، لكنهم فشلوا في متابعة رد الفعل لأنهم لم يتمكنوا من بلورة وتوصيف المنتجات الراتنجية غير المتبلورة. كان Baekeland هو الذي نجح في عام 1907 في التحكم في تفاعل التكثيف لإنتاج أول راتنج صناعي. كان Baekeland قادرًا على إيقاف التفاعل بينما كان الراتنج لا يزال في حالة قابلة للانصهار وقابلة للذوبان (المرحلة A) ، حيث يمكن إذابته في مذيبات وخلطه مع مواد مالئة وتعزيزات من شأنها أن تجعله من البلاستيك القابل للاستخدام. ثم تم إحضار الراتينج ، في هذه المرحلة المسماة ريسول ، إلى المرحلة ب ، حيث ، على الرغم من أنه غير قابل للذوبان تقريبًا وغير قابل للذوبان ، فإنه لا يزال يمكن تليينه بالحرارة إلى الشكل النهائي في القالب. كانت درجة الحرارة الحرارية التي تم علاجها بالكامل هي المرحلة C. في عام 1911 ، بدأت شركة Bakelite العامة في Baekeland عملياتها في Perth Amboy ، NJ ، الولايات المتحدة ، وبعد ذلك بوقت قصير كانت العديد من الشركات تستخدم منتجات البلاستيك الباكليت. في سوق البلاستيك التي تحتكرها فعليًا مادة السيليلويد ، وهي مادة قابلة للاشتعال للغاية تذوب بسهولة وتلين بالحرارة ، وجد الباكليت قبولًا جاهزًا لأنه يمكن أن يصبح غير قابل للذوبان وغير قابل للانغلاق. علاوة على ذلك ، سيتحمل منتج التسخين الحراري كميات كبيرة من المكونات الخاملة ، وبالتالي يمكن تعديله من خلال دمج مواد مالئة مختلفة ، مثل دقيق الخشب وقطيع القطن والأسبستوس والنسيج المفروم. نظرًا لخصائصه العازلة الممتازة ، تم تصنيع الراتنج في مقابس ومقابض وأقراص للراديو وتم استخدامه في الأنظمة الكهربائية للسيارات.
يتم استخدام طريقتين لصنع بوليمرات الفينول فورمالدهايد. في أحدها ، يتم تفاعل فائض من الفورمالديهايد مع الفينول في وجود محفز أساسي في محلول مائي لإنتاج المحلول ، وهو بوليمر أولي منخفض الوزن الجزيئي مع مجموعات CH 2 OH مرتبطة بحلقات الفينول. عند التسخين ، يتكثف المزيج بشكل أكبر ، مع فقدان الماء والفورمالديهايد ، لإنتاج بوليمرات شبكة بالحرارة. تتضمن الطريقة الأخرى تفاعل الفورمالديهايد مع فائض من الفينول باستخدام محفز حمض لإنتاج بوليمرات أولية تسمى نوفولاك. تشبه Novolacs البوليمر إلا أنها ذات وزن جزيئي أقل بكثير ولا تزال بلاستيكية حرارية. يتم تحقيق المعالجة لشبكة البوليمر عن طريق إضافة المزيد من الفورمالديهايد أو ، بشكل أكثر شيوعًا ، من المركبات التي تتحلل إلى الفورمالديهايد عند التسخين.
تصنع بوليمرات الفينول فورمالدهايد مواد لاصقة خشبية ممتازة للخشب الرقائقي والألواح الحبيبية لأنها تشكل روابط كيميائية مع مكون اللجنين الفينوليكي للخشب. في الواقع ، تمثل المواد اللاصقة للخشب أكبر سوق لهذه البوليمرات. تكون البوليمرات داكنة اللون نتيجة للتفاعلات الجانبية أثناء البلمرة. نظرًا لأن لونها يلطخ الخشب كثيرًا ، فهي ليست مناسبة للألواح الزخرفية الداخلية. إنها المادة اللاصقة المفضلة للخشب الرقائقي الخارجي ، نظرًا لمقاومتها الجيدة للرطوبة.
راتنجات الفينول ، التي يتم تعزيزها دائمًا بالألياف أو الرقائق ، مصبوبة أيضًا في أجسام مقاومة للحرارة مثل الموصلات الكهربائية ومقابض الأجهزة.
بوليمرات اليوريا فورمالدهايد
بدأت الراتنجات المصنوعة من بوليمرات اليوريا فورمالدهايد الاستخدام التجاري في المواد اللاصقة والمجلدات في عشرينيات القرن العشرين. يتم معالجتها بنفس الطريقة التي تتم بها إعادة معالجة المواد (أي استخدام الفورمالديهايد الزائد). مثل الفينولات ، تُستخدم البوليمرات كمادة لاصقة للخشب ، ولكن لأنها أخف في اللون ، فهي أكثر ملاءمة للخشب الرقائقي الداخلي والألواح الزخرفية. ومع ذلك ، فهي أقل متانة ، ولا تتمتع بمقاومة كافية للطقس لاستخدامها في التطبيقات الخارجية.
كما تستخدم بوليمرات اليوريا فورمالدهايد لعلاج ألياف النسيج من أجل تحسين مقاومة التجاعيد والتقلص ، وتمزج مع دهانات الألكيد من أجل تحسين صلابة السطح.
بوليمرات الميلامين فورمالدهايد
هذه المركبات تشبه راتنجات اليوريا فورمالدهايد في معالجتها وتطبيقاتها. بالإضافة إلى ذلك ، فإن صلابة أكبر ومقاومة للماء تجعلها مناسبة لأواني الطعام الزخرفية وتصنيعها في سطح الطاولة ومنتجات كونترتوب التي طورتها شركة Formica وتم بيعها تحت الاسم التجاري Formica.
كما تم استخدام البوليمرات القائمة على الميلامين على نطاق واسع كعوامل ربط متصالب في أنظمة طلاء السطح المخبوزة. على هذا النحو ، كان لديهم العديد من التطبيقات الصناعية - على سبيل المثال ، في معاطف السيارات والتشطيبات للأثاث والأثاث المعدني. ومع ذلك ، فإن استخدامها في الطلاء يتناقص بسبب القيود المفروضة على انبعاث الفورمالديهايد ، وهو مكون رئيسي في هذه الطلاءات.
السليلوزات
السليلوز (C 6 H 7 O 2 [OH] 3) هو بوليمر يحدث بشكل طبيعي ويتكون من وحدات الجلوكوز المتكررة. في حالتها الطبيعية (المعروفة باسم السليلوز الأصلي) ، تم حصادها منذ فترة طويلة كألياف تجارية - كما هو الحال في القطن والكتان والقنب والكابوك والسيزال والجوت والرامي. الخشب ، الذي يتكون من السليلوز بالاشتراك مع بوليمر شبكة معقد يسمى اللجنين ، هو مادة بناء شائعة. يتم تصنيع الورق أيضًا من السليلوز الأصلي. على الرغم من أنه بوليمر خطي ، إلا أن السليلوز يعمل بالحرارة. بمعنى أنه يشكل هياكل دائمة ومترابطة لا يمكن فكها بالحرارة أو المذيبات دون التسبب في التحلل الكيميائي. ينشأ سلوكها بالحرارة من عوامل الجذب ثنائية القطب القوية الموجودة بين جزيئات السليلوز ، مما يضفي خصائص مشابهة لتلك الموجودة في بوليمرات الشبكة المترابطة.
في القرن التاسع عشر ، تم تطوير طرق لفصل السليلوز الخشبي عن اللجنين كيميائيًا ثم تجديد السليلوز مرة أخرى إلى تكوينه الأصلي لاستخدامه في كل من الألياف (الرايون) والبلاستيك (السيلوفان). كما تم تطوير مشتقات الإستر والأثير للسليلوز واستخدامها كألياف ومواد بلاستيكية. كانت المركبات الأكثر أهمية هي نترات السليلوز (نيتروسليلوز ، مصنوعة في مادة سيلولويد) وأسيتات السليلوز (المعروفة سابقًا باسم رايون خلات ولكنها تعرف الآن ببساطة باسم خلات). استند كل من هذه المشتقات الكيميائية إلى بنية السليلوز
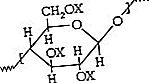
مع كون X NO 2 في حالة النترات و COCH 3 في حالة الأسيتات.














