المعدن الانتقالي ، أي من العناصر الكيميائية المختلفة التي تحتوي على إلكترونات تكافؤ - أي إلكترونات يمكن أن تشارك في تكوين الروابط الكيميائية - في قوقعتين بدلاً من واحدة فقط. في حين أن مصطلح الانتقال ليس له أهمية كيميائية معينة ، فهو اسم مناسب يميز من خلاله تشابه الهياكل الذرية والخصائص الناتجة للعناصر المعينة على هذا النحو. يشغلون الأجزاء الوسطى من الفترات الطويلة للجدول الدوري للعناصر بين المجموعات الموجودة على الجانب الأيسر والمجموعات الموجودة على اليمين. على وجه التحديد ، يشكلون المجموعات 3 (IIIb) حتى 12 (IIb).
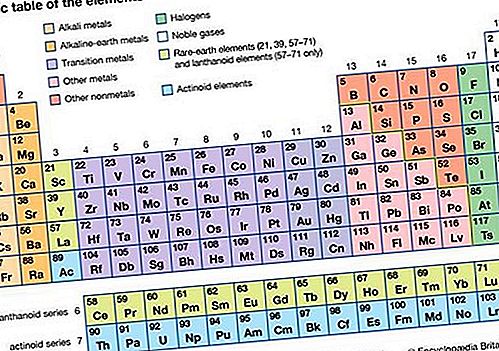
الخصائص العامة للمجموعة
أكثر أوجه التشابه اللافتة بين العناصر الـ 24 المعنية هي أنها كلها معادن وأن معظمها صلب وقوي ولامع ولديه نقاط انصهار وغليان عالية ، وهو موصل جيد للحرارة والكهرباء. النطاق في هذه الخصائص كبير. وبالتالي فإن العبارات تكون مقارنة مع الخصائص العامة لجميع العناصر الأخرى.
العديد من العناصر ذات أهمية تكنولوجية: التيتانيوم والحديد والنيكل والنحاس ، على سبيل المثال ، يتم استخدامها هيكليًا وفي التكنولوجيا الكهربائية. ثانيًا ، تشكل الفلزات الانتقالية العديد من السبائك المفيدة ، مع بعضها البعض ومع العناصر المعدنية الأخرى. ثالثًا ، تذوب معظم هذه العناصر في الأحماض المعدنية ، على الرغم من أن القليل منها ، مثل البلاتين والفضة والذهب ، يطلق عليها "النبيل" - أي أنها لا تتأثر بالأحماض البسيطة (غير المؤكسدة).
بدون استثناء ، تشكل عناصر سلسلة الانتقال الرئيسية (على سبيل المثال ، باستثناء اللانثينويد والأكتينيدات على النحو المحدد أدناه) مركبات مستقرة في حالتي أكسدة رسمية أو أكثر.
يمكن تقسيم المعادن الانتقالية وفقًا للبنى الإلكترونية لذراتها إلى ثلاث سلاسل انتقالية رئيسية ، تسمى سلسلة الانتقال الأولى والثانية والثالثة ، وسلسلتان انتقاليتان داخليتان ، تسمى اللانثانويد والأكتينيدات.
تبدأ السلسلة الانتقالية الرئيسية الأولى إما سكانديوم (الرمز Sc ، العدد الذري 21) أو التيتانيوم (الرمز Ti ، العدد الذري 22) وتنتهي بالزنك (الرمز Zn ، العدد الذري 30). تتضمن السلسلة الثانية العناصر yttrium (الرمز Y ، العدد الذري 39) إلى الكادميوم (الرمز Cd ، العدد الذري 48). تمتد السلسلة الثالثة من اللانثانم (الرمز La ، العدد الذري 57) إلى الزئبق (الرمز Hg ، العدد الذري 80). يتم تضمين سلسلة الانتقال الرئيسية الثلاثة هذه في مجموعة من 30 عنصرًا تسمى غالبًا معادن الانتقال d-block. نظرًا لأن scandium و yttrium و lanthanum لا تشكل في الواقع مركبات مماثلة لتلك الموجودة في المعادن الانتقالية الأخرى ولأن كيمياءها متجانسة تمامًا مع تلك الموجودة في اللانثينيدات ، يتم استبعادها من المناقشة الحالية للمعادن الانتقالية الرئيسية. وبالمثل ، لأن الزنك والكادميوم والزئبق لا يظهران إلا القليل من الخصائص المميزة للمعادن الانتقالية الأخرى ، يتم معالجتها بشكل منفصل (انظر عنصر مجموعة الزنك). يتم سرد المعادن الانتقالية لبقية d- وبعض خصائصها المميزة في الجدول.
بعض خصائص العناصر الانتقالية
| رمز | العدد الذري | الكتلة الذرية | الكثافة (جرام لكل سنتيمتر مكعب ، 20 درجة مئوية) | نقطة انصهار (درجة مئوية) | نقطة الغليان (درجة مئوية) | ||
|---|---|---|---|---|---|---|---|
| السلسلة الرئيسية الأولى | التيتانيوم | Ti | 22 | 47.867 | 4.54 | 1،668 | 3،287 |
| الفاناديوم | الخامس | 23 | 50.942 | 6.11 | 1،910 | 3،407 | |
| الكروم | سجل تجاري | 24 | 51.996 | 7.14 | 1،907 | 2،672 | |
| المنغنيز | Mn | 25 | 54.938 | 7.21-7.44 | 1،246 | 2،061 | |
| حديد | Fe | 26 | 55.845 | 7.87 | 1،538 | 2861 | |
| الكوبالت | Co | 27 | 58.933 | 8.9 | 1،495 | 2،927 | |
| النيكل | ني | 28 | 58.693 | 8.9 | 1،455 | 2،913 | |
| نحاس | النحاس | 29 | 63.546 | 8.92 | 1،085 | 2،927 | |
| السلسلة الرئيسية الثانية | الزركونيوم | Zr | 40 | 91.224 | 6.51 | 1،855 | 4،409 |
| النيوبيوم | ملحوظة | 41 | 92.906 | 8.57 | 2،477 | 4،744 | |
| الموليبدينوم | مو | 42 | 95.94 | 10.22 | 2،623 | 4639 | |
| التكنيتيوم | ح | 43 | 98 | 11.5 | 2،157 | 4،265 | |
| الروثنيوم | رو | 44 | 101.07 | 12.41 | 2334 | 4،150 | |
| الروديوم | Rh | 45 | 102.906 | 12.41 | 1،964 | 3،695 | |
| البلاديوم | ص | 46 | 106.42 | 12.02 | 1،555 | 2،963 | |
| فضة | اي جي | 47 | 107.868 | 10.49 | 962 | 2،162 | |
| السلسلة الرئيسية الثالثة | الهافنيوم | Hf | 72 | 178.49 | 13.31 | 2،233 | 4،603 |
| التنتالوم | تا | 73 | 180.948 | 16.65 | 3،017 | 5،458 | |
| التنغستن | دبليو | 74 | 183.84 | 19.3 | 3،422 | 5،555 | |
| الرينيوم | إعادة | 75 | 186.207 | 21.02 | 3،186 | 5،596 | |
| الأوزميوم | Os | 76 | 190.23 | 22.57 | 3،033 | 5،012 | |
| إيريديوم | Ir | 77 | 192.217 | 22.56 | 2،446 | 4،428 | |
| البلاتين | نقطة | 78 | 195.084 | 21.45 | 1،768 | 3825 | |
| ذهب | Au | 79 | 196.967 | ~ 19.3 | 1،064 | 2856 |
يتضمن أول سلسلة الانتقال الداخلي العناصر من السيريوم (الرمز Ce ، العدد الذري 58) إلى اللوتيتيوم (الرمز Lu ، العدد الذري 71). تسمى هذه العناصر اللانثينيدات (أو اللانثينيدات) لأن كيمياء كل منها تشبه إلى حد كبير اللانثانم. غالبًا ما يُنظر إلى اللانثانم نفسه على أنه أحد اللانثينيدات. تتكون سلسلة الأكتينويد من 15 عنصرًا من الأكتينيوم (الرمز Ac ، العدد الذري 89) إلى lawrencium (الرمز Lr ، العدد الذري 103). هذه السلسلة الانتقالية الداخلية مغطاة تحت عنصر الأرض النادرة والعنصر الأكتيني. للعناصر 104 وما فوق ، انظر عنصر ما وراء اليورانيوم.
يمكن فهم المواقع النسبية للمعادن الانتقالية في الجدول الدوري وخصائصها الكيميائية والفيزيائية بشكل أفضل من خلال النظر في الهياكل الإلكترونية والطريقة التي تختلف بها هذه الهياكل مع زيادة الأعداد الذرية.
المدارات الذرية لذرة الهيدروجين
كما ذكرنا سابقًا ، فإن الإلكترونات المرتبطة بنواة ذرية موضعية ، أو مركزة ، في مناطق محددة مختلفة من الفضاء تسمى المدارات الذرية ، وتتميز كل منها بمجموعة من الرموز (الأرقام الكمومية) التي تحدد الحجم والشكل و التوجه في الفضاء بالنسبة إلى المدارات الأخرى. قد لا يستوعب المدار أكثر من إلكترونين. يتم تحديد الطاقة المتضمنة في تفاعل الإلكترون مع النواة من خلال المدار الذي تشغله ، وتوزع الإلكترونات في الذرة نفسها بين المدارات بطريقة تجعل الطاقة الإجمالية هي الحد الأدنى. وهكذا ، عن طريق التركيب الإلكتروني ، أو التكوين ، للذرة يعني الطريقة التي تشغل بها الإلكترونات المحيطة بالنواة مختلف المدارات الذرية المتاحة لها. أبسط تكوين هو مجموعة مدارات إلكترون واحد لذرة الهيدروجين. يمكن تصنيف المدارات ، أولاً ، من خلال العدد الكمي الرئيسي ، وللمدارات طاقة متزايدة مع زيادة العدد الكمي الرئيسي من 1 إلى 2 ، 3 ، 4 ، إلخ. (مجموعات المدارات المحددة بأرقام الكم الرئيسية 1 ، 2 ، 3 ، 4 ، وما إلى ذلك ، وغالبًا ما يشار إليها على أنها قذائف تسمى K ، L ، M ، N ، إلخ.) بالنسبة للرقم الكمي الأساسي 1 لا يوجد سوى نوع واحد من المدارات ، يسمى المدار s. مع زيادة العدد الكمي الرئيسي ، هناك عدد متزايد من الأنواع المختلفة من المدارات ، أو القذائف الفرعية ، المقابلة لكل منها: s ، p ، d ، f ، g ، إلخ. علاوة على ذلك ، تأتي الأنواع المدارية الإضافية في مجموعات أكبر. وبالتالي ، لا يوجد سوى مدار واحد لكل عدد كمي رئيسي ، ولكن هناك ثلاثة مدارات في المجموعة المعينة p ، وخمسة في كل مجموعة معينة d ، وما إلى ذلك. بالنسبة لذرة الهيدروجين ، يتم تحديد الطاقة بشكل كامل من خلال المدار الذي يشغله الإلكترون المفرد. من الجدير بالملاحظة بشكل خاص أن طاقة ذرة الهيدروجين يتم تحديدها فقط من خلال العدد الكمي الرئيسي للمدار الذي يشغله الإلكترون (باستثناء بعض التأثيرات الصغيرة التي لا تثير القلق هنا) ؛ أي ، في الهيدروجين ، تكون تكوينات الإلكترون للقشرة الثالثة ، على سبيل المثال ، متساوية الطاقة (من نفس الطاقة ، أيهما يشغلها الإلكترون) ، وهو ليس هو الحال مع أي من الذرات الأخرى ، وكلها تحتوي على إلكترونين أو أكثر.
المدارات الذرية لذرات متعددة الإلكترونات
لفهم تكوينات الإلكترونات للذرات الأخرى ، من المعتاد استخدام مبدأ Aufbau (الألماني: "البناء") ، والذي أساسه أنه لتحقيق تكوين متعدد الإلكترونات ، يجب إضافة العدد المطلوب من الإلكترونات إلى المدارات واحدة تلو الأخرى ، وملء المدارات الأكثر استقرارًا أولاً ، حتى تمت إضافة العدد الإجمالي. وهكذا ، في "بناء" الجدول الدوري ، يتقدم المرء من عنصر إلى آخر بإضافة بروتون واحد إلى النواة وإلكترون واحد إلى المنطقة الذرية خارج النواة. هناك قيد واحد على هذا المفهوم ، وهو مبدأ استبعاد باولي ، الذي ينص على أن إلكترونين فقط قد يشغلان كل مدار. وبالتالي لا يمكن أن يكون هناك أكثر من إلكترونين في أي مدار s ، وستة إلكترونات في أي مجموعة من المدارات p ، وعشرة إلكترونات في أي مجموعة من المدارات d ، وما إلى ذلك. عند تنفيذ هذه العملية ، لا يمكن للمرء ببساطة استخدام ترتيب الإلكترون المدارات المناسبة لذرة الهيدروجين. عند إضافة الإلكترونات فإنها تتفاعل مع بعضها البعض وكذلك مع النواة ، ونتيجة لذلك فإن وجود الإلكترونات في بعض المدارات يجعل طاقة الإلكترون الذي يدخل مدارًا آخر مختلفًا عما سيكون عليه إذا كان هذا الإلكترون موجودًا بمفرده. النتيجة الإجمالية لهذه التفاعلات بين الإلكترونيات (يشار إليها أحيانًا باسم التدريع) هي أن الترتيب النسبي لمختلف المدارات الذرية يختلف في العديد من ذرات الإلكترون عن ذرات الهيدروجين ؛ في الواقع ، يتغير باستمرار مع زيادة عدد الإلكترونات.
عندما يتم بناء الذرات متعددة الإلكترونيات ، تتوقف الأفرع الفرعية المختلفة s و p و d و f و g وما إلى ذلك من العدد الكمي الرئيسي عن كونها متساوية الطاقة ؛ تنخفض جميعها ، على الرغم من أنه ليس بكميات متساوية ، إلى طاقات أقل. يحدث انخفاض الطاقة بشكل عام لأن الحماية من الشحنة النووية التي يعطاها الإلكترون في مدار معين من قبل جميع الإلكترونات الأخرى في الذرة ليست كافية لمنع الزيادة المطردة في تأثير الشحنة في النواة على ذلك الإلكترون مع زيادة العدد الذري. بعبارة أخرى ، كل إلكترون محمي بشكل غير كامل من الشحنة النووية بواسطة الإلكترونات الأخرى. بالإضافة إلى أنواع مختلفة من المدارات في كل قذيفة رئيسية ، بسبب توزيعاتها المكانية المختلفة ، يتم حمايتها بدرجات مختلفة بواسطة قلب الإلكترونات تحتها ؛ وفقًا لذلك ، على الرغم من انخفاضها جميعًا في الطاقة ، إلا أنها تنخفض بمقادير مختلفة ، وبالتالي يتغير ترتيبها النسبي في الطاقة باستمرار. من أجل تحديد التكوين الإلكتروني لذرة معينة ، من الضروري استخدام ترتيب المدارات المناسبة للقيمة المحددة للعدد الذري لتلك الذرة. يجب ملاحظة سلوك مختلف المدارات d و f بشكل خاص فيما يتعلق بمكان حدوث المعادن الانتقالية في الجدول الدوري.
ذرة الأرجون (العدد الذري 18) لها تكوين إلكترون 1s 2 2s 2 2p 6 3s 2 3p 6 (أي أنها تحتوي على إلكترونين في المدار s للقشرة الأولى ؛ اثنان في s وستة في مدارات p الصدفة الثانية ؛ اثنان في s وستة في مدارات p من القشرة الثالثة: غالبًا ما يتم اختصار هذا التعبير [Ar] خاصة في تحديد تكوينات العناصر بين الأرجون والكريبتون ، لأنها تمثل جزءًا مشتركًا من تكوينات كل هذه عناصر). المدارات ثلاثية الأبعاد محمية أكثر من الشحنة النووية من المدارات الأربعة ، وبالتالي فإن المدار الأخير لديه طاقة أقل. تدخل الإلكترونات التالية التي سيتم إضافتها إلى مدار 4s بشكل مفضل على مدارات 3d أو 4p. العنصران التاليان للأرجون في الجدول الدوري هما البوتاسيوم ، مع إلكترون 4s واحد ، والكالسيوم ، مع إلكترون 4s. نظرًا لوجود إلكترونات 4s ، تكون المدارات ثلاثية الأبعاد أقل حماية من المدارات 4p ؛ لذلك ، تبدأ سلسلة الانتقال المنتظمة الأولى عند هذه النقطة مع عنصر scandium ، الذي له تكوين الإلكترون [Ar] 4s 2 3d 1. من خلال العناصر التسعة التالية ، بترتيب متزايد من العدد الذري ، تتم إضافة الإلكترونات إلى المدارات ثلاثية الأبعاد حتى يتم ملءها بالكامل في عنصر الزنك ويكون تكوين الإلكترون [Ar] 3d 10 4s 2. بعد ذلك ، تكون مدارات 4p هي الأقل طاقة ، وتصبح ممتلئة من خلال العناصر الستة التالية ، سادسها هو الغاز النبيل التالي ، الكريبتون ، مع تكوين الإلكترون 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 أو [Kr].
طوال الفترة التالية ، يشبه نمط اختلاف الطاقات المدارية ذلك الذي يسبق مباشرة. عندما يتم تحقيق تكوين الغاز النبيل ، الكريبتون ، يكون المدار 5s أكثر استقرارًا من المدارات 4d. وبالتالي يدخل الإلكترونان التاليان في المدار 5s ، ولكن بعد ذلك تنخفض المدارات 4d إلى طاقة أقل من المدارات 5p ، وتبدأ سلسلة الانتقال العادية الثانية مع عنصر الإيتريوم. تستمر إضافة الإلكترونات إلى المدارات 4d حتى تمتلئ هذه المدارات تمامًا في موقع عنصر الكادميوم ، الذي يحتوي على تكوين إلكترون [Kr] 4d 10 5s 2. تدخل الإلكترونات الستة التالية إلى المدارات 5p حتى يتم الوصول إلى تكوين غاز نبيل آخر في عنصر زينون. وبالمقارنة مع الفترتين السابقتين ، تتم إضافة الإلكترونين التاليين إلى المدار المتاح التالي ، وهما المدار 6s ، وينتج عنهما العنصران التاليان ، السيزيوم والباريوم. في هذه المرحلة ، ومع ذلك ، يصبح ترتيب المدارات أكثر تعقيدًا مما كان عليه سابقًا ، نظرًا لوجود مدارات 4f غير مملوءة بالإضافة إلى المدارات 5d ، وللمجموعتين نفس الطاقة تقريبًا. في العنصر التالي ، lanthanum (العدد الذري 57) ، يضاف إلكترون إلى المدارات 5d ، ولكن العنصر التالي مباشرة ، السيريوم (العدد الذري 58) ، يحتوي على إلكترونين في مدارات 4f ولا يوجد في المدارات 5d. من خلال العناصر الـ 12 التالية ، تدخل الإلكترونات الإضافية إلى مدارات 4f ، على الرغم من أن المدارات 5d لها طاقة أعلى قليلاً فقط. هذه المجموعة من العناصر ، التي تمتد من اللانثانم ، حيث لا تزال مدارات 4f شاغرة أو على وشك أن يتم ملؤها ، من خلال اللوتيتيوم ، حيث يتم ملء مدارات 4f بالكامل بواسطة 14 إلكترونًا ، تشكل اللانثانويدات المذكورة أعلاه.
عند هذه النقطة ، تكون المدارات المتاحة التالية هي المدارات 5d ، والعناصر hafnium من خلال الذهب ، سلسلة الانتقال العادية الثالثة ، تتوافق مع التعبئة المتتالية لهذه المدارات 5d. بعد هذه السلسلة ، هناك مرة أخرى مدارات p (6p) يجب ملؤها ، وعندما يتحقق ذلك يتم الوصول إلى غاز الرادون النبيل.













